Với bài bác tập chuỗi phản bội ứng chất hóa học hợp hóa học vô cơ và bí quyết giải môn Hóa lớp 9 gồm cách thức giải bỏ ra tiết, bài xích tập minh họa có giải thuật và bài bác tập từ luyện để giúp đỡ học sinh biết cách làm bài xích tập bài tập chuỗi làm phản ứng hóa học hợp hóa học vô cơ. Mời các bạn đón xem:
Bài tập chuỗi phản nghịch ứng chất hóa học hợp hóa học vô cơ và phương pháp giải - Hóa lớp 9
I. Kim chỉ nan và cách thức giải
Dạng bài bác này tất cả một chuỗi các phản ứng hóa học đề xuất yêu cầu học sinh phải thế chắc sơ đồ, cũng tương tự mối contact giữa những hợp chất vô cơ, ráng thể:
a/ Sơ đồ những loại hợp chất vô cơ:
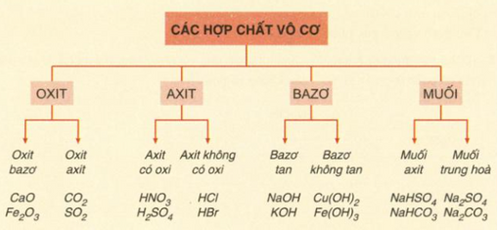
b/ Sơ vật dụng mối tương tác giữa các chất vô cơ:
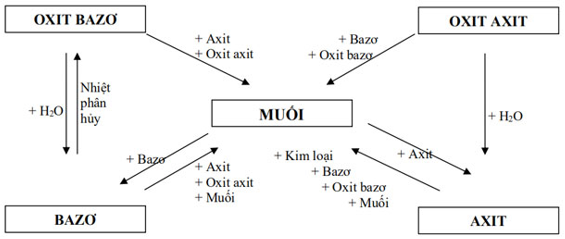
Các bước hoàn thành chuỗi làm phản ứng:
- cách 1: Xác định đúng đắn các chất trong chuỗi (nếu chuỗi bội phản ứng hóa học ẩn chất).
Bạn đang xem: Chuỗi phản ứng hóa học lớp 8
- bước 2: Viết phương trình làm phản ứng hóa học.
II. Ví dụ như minh họa
Ví dụ 1: xong xuôi chuỗi bội phản ứng sau:
SO2→ SO3→ H2SO4→ Zn
SO4→ Zn(OH)2→ Zn
O
Hướng dẫn giải:
1) 2SO2+ O2→to2SO3
2) SO3+ H2O → H2SO4
3) H2SO4+Zn → Zn
SO4+ H2
4) Zn
SO4 dư+ 2Na
OH → Zn(OH)2↓ + Na2SO4
5) Zn(OH)2→to
Zn
O + H2O
Ví dụ 2: xong xuôi chuỗi làm phản ứng sau cùng viết phương trình làm phản ứng hóa học:
Ca→+O2A→+H2OB→+CO2C
Hướng dẫn giải:
Các hóa học A, B, C lần lượt là:
Ca→(1)+O2Ca
O→(2)+H2OCa(OH)2→(3)+CO2Ca
CO3
Các phương trình bội phản ứng hóa học:
(1) 2Ca + O2 →To2Ca
O
(2) Ca
O + H2O → Ca(OH)2
(3) Ca(OH)2 + CO2 → Ca
CO3 ↓ + H2O
III. Bài tập từ bỏ luyện
Bài 1:
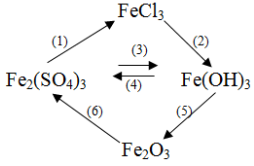
Viết phương trình bội nghịch ứng hóa học đến chuỗi làm phản ứng trên.
Hướng dẫn giải:
(1)Fe2(SO4)3+ 3Ba
Cl2→ 3Ba
SO4↓ + 2Fe
Cl3
(2)Fe
Cl3+ 3Na
OH → Fe(OH)3↓ + 3Na
Cl
(3)Fe2(SO4)3+ 6Na
OH → 2Fe(OH)3↓ + 3Na2SO4
(4)2Fe(OH)3+ 3H2SO4→ Fe2(SO4)3+ 6H2O
(5) 2Fe(OH)3→to
Fe2O3 + 3H2O
(6)Fe2O3+ 3H2SO4→ Fe2(SO4)3+ 3H2O
Bài 2: kết thúc chuỗi phản nghịch ứng sau:
Na → Na2O → Na
OH → Na2CO3→ Na
Cl → Na
OH → Na
HCO3
Hướng dẫn giải:
1) 4Na + O2→to2Na2O
2) Na2O + H2O → 2Na
OH
3) 2Na
OH + CO2→ Na2CO3+ H2O
4) Na2CO3+ 2HCl → 2Na
Cl + CO2+ H2O
5) 2Na
Cl + H2O →dpdd2Na
OH + H2+ Cl2
6) Na
OH + CO2→ Na
HCO3
Bài 3: Viết phương trình phản ứng hóa học cho chuỗi phản bội ứng sau:
Mg
CO3 → Mg
SO4 → Mg
Cl2 → Mg(OH)2 → Mg
O → Mg
SO4.
Hướng dẫn giải:
(1) Mg
CO3 + H2SO4 → Mg
SO4 + CO2 + H2O
(2) Mg
SO4 + Ba
Cl2 → Mg
Cl2 + Ba
SO4↓
(3) Mg
Cl2 + 2Na
OH → Mg(OH)2 ↓ + 2Na
Cl
(4) Mg(OH)2 →to
Mg
O + H2O
(5) Mg
O + H2SO4 → Mg
SO4 + H2O
Bài 4:
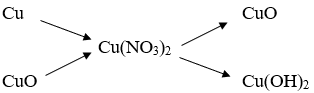
Viết phương trình phản bội ứng hóa học cho chuỗi bội phản ứng trên.
Hướng dẫn giải:
(1) Cu + 4HNO3 → Cu(NO3)2 + 2NO2 + 2H2O
(2) Cu
O + 2HNO3 → Cu(NO3)2 + H2O
(3) 2Cu(NO3)2 →to2Cu
O + 4NO2 + O2
(4) Cu(NO3)2 + 2Na
OH → Cu(OH)2 + 2Na
NO3
Bài 5:
Fe
S2 + O2 →to
A + B
A + O2 →to
C
C + D → Axit E
E + Cu → F + A + D
A + D → Axit G
Xác định A, B, C, D, E, F, G và hoàn thành các phương trình làm phản ứng chất hóa học trên.
Hướng dẫn giải:
(1) 4Fe
S2 + 11O2 →to8SO2 + 2Fe2O3
(2) 2SO2 + O2 →to,V2O52SO3
(3) SO3 + H2O → H2SO4
(4) 2H2SO4 + Cu → Cu
SO4 + SO2 + 2H2O
(5) SO2 + H2O → H2SO3
A: SO2
B: Fe2O3
C: SO3
D: H2O
E: H2SO4
F: Cu
SO4
G: H2SO3
Bài 6:
? + ? → Ca
CO3 ↓ + ?
Al2O3 + H2SO4 → ? + ?
Na
Cl + ? → ? + ? + Na
OH
KHCO3 + Ca(OH)2 → ? + ? + ?
Hướng dẫn giải:
(1) Na2CO3 + Ca(OH)2 → Ca
CO3↓ + 2Na
OH
(2) Al2O3 + 3H2SO4 → Al2(SO4)3 + 3H2O
(3) 2Na
Cl + 2H2O →đpdd2Na
OH + H2 + Cl2
(4) 2KHCO3 + Ca(OH)2 → Ca
CO3↓ + K2CO3 + 2H2O
Bài 7: Viết phương trình phản nghịch ứng hóa học mang lại chuối làm phản ứng sau:
Al → Al2O3→ Na
Al
O2→Al(OH)3→ Al2(SO4)3→ Al
Cl3→ Al(NO3)3
Hướng dẫn giải:
1) 4Al + 3O2→to2Al2O3
2) Al2O3+ 2Na
OH → 2Na
Al
O2+ H2O
3) 2Na
Al
O2+ CO2 + 3H2O → Na2CO3 + 2Al(OH)3↓
4) 2Al(OH)3 + 3H2SO4 → Al2(SO4)3 + 6H2O
5) Al2(SO4)3+ 3Ba
Cl2→ 2Al
Cl3+ 3Ba
SO4↓
6) Al
Cl3+ 3Ag
NO3→ Al(NO3)3+ 3Ag
Cl↓
Bài 8: hoàn thành sơ đồ phản ứng sau:
Mn
O2→+X,to
Cl2 →+B,to
HCl →+H2OX →+CFe
Cl2 + Fe
Cl3
Hướng dẫn giải:
1) Mn
O2 + 4HCl →to
Mn
Cl2 + Cl2 + 2H2O
(2) Cl2 + H2 →to2HCl(k)
(3) HCl (k) + H2O → dd HCl
(4) 8HCl + Fe3O4 → Fe
Cl2 + 2Fe
Cl3 + 4H2O
B: H2
C: Fe3O4
X: HCl
Bài 9: Thay các chữ chiếc bằng những công thức hóa học phù hợp và chấm dứt các phản ứng sau:
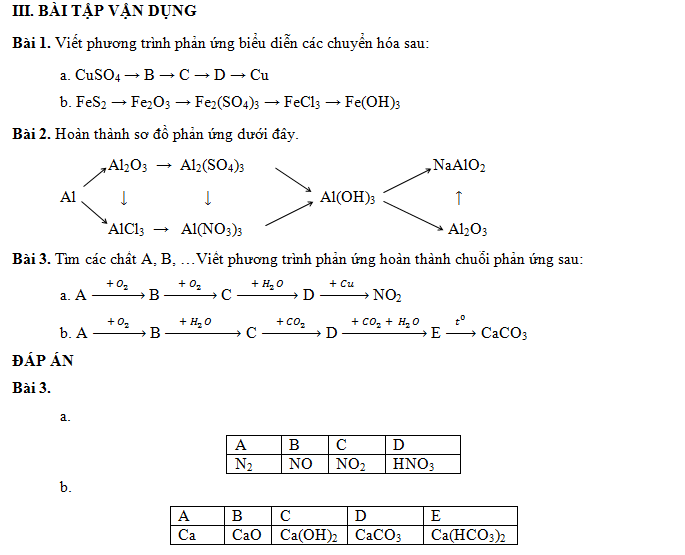
Bài tập chuỗi bội phản ứng hóa học góp học sinh cải thiện khả năng bốn duy xúc tích và ngắn gọn đồng thời tương khắc sâu kỹ năng hóa học tập trọng tâm.
Tính chất, ứng dụng của Hiđro

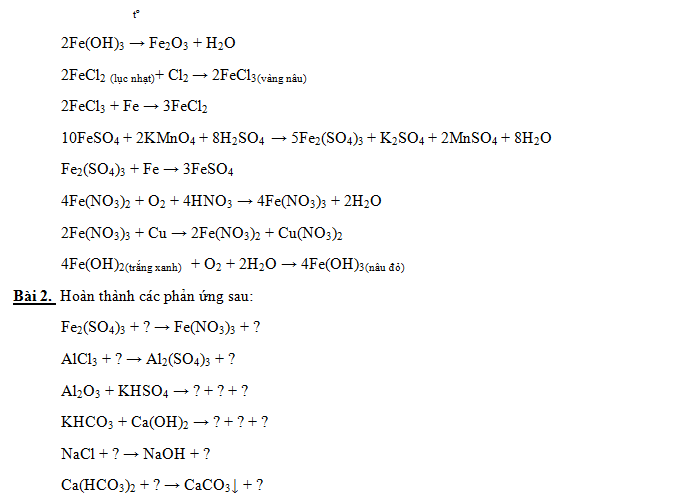
BT chuỗi phản bội ứng hóa học



BT chuỗi làm phản ứng hóa học
Hiđro bao gồm ứng dụng quan trọng trong đời sống hàng ngày. Vậy hiđro gồm những đặc thù nào????
TÍNH CHẤT VÀ ỨNG DỤNG CỦA HIĐRO




Bài 1. những phương trình phản ứng chất hóa học nào sau đó là phản ứng lão hóa khử:
a. Teo + O2 → CO2
b. Al + Fe2O3 → Al2O3 + Fe
c. Mg + CO2 → Mg
O + CO
d. Co + H2O → CO2 +H2
e. Ca
O + H2O → Ca(OH)2
và thăng bằng phản ứng thoái hóa khử, cho biết thêm chất oxi hóa, hóa học khử
Bài 2. Phân biệt các loại chất bao gồm công thức hóa học sau:
HCl; Ca
O; Cu(OH)2; Fe; S; Na; P; P2O5; SO3; Na
HCO3; KOH; KNO3; H2SO4.
Bài 3. Các chất nào tiếp sau đây điều chế hiđro
A. H2O; HCl ; H2SO4
B. HNO3; H3PO4; Na
HCO3
C. Ca
CO3; Ca(HCO3)2; KCl
O3
D. NH4Cl; KMn
O4; KNO3
Hãy chọn giải đáp đúng.
Bài 4. Các hóa học nào dưới đây có thể chức năng được với nhau? Hãy viết phương trình bội phản ứng đó:
H2; Al2O3; Fe
O; SO2; P2O5; K; H2O
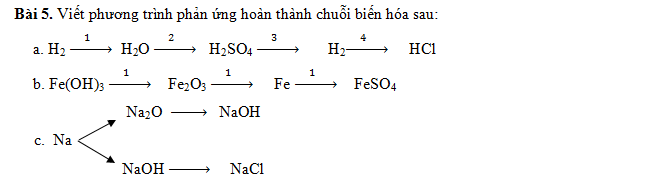
Bài 6. Một học sinh làm thí nghiệm như sau:
a. Nung nóng can xi cacbonat.
b. Cho một cây đinh sắt vào lọ đựng dung dịch đồng sunfat, sau một thời gian có vết màu đỏ bám vào cây đinh.
c. Dẫn khí hiđro đi qua chì (II) oxit nung nóng.
d. Đốt cháy một mẩu than
Các phân tích trên thuộc loại phản ứng chất hóa học nào sau đây?
A. Phản ứng thoái hóa – khử
B. Phản bội ứng hóa hợp
C. Phản bội ứng phân hủy
D. Phản bội ứng thế
E. Tất cả các làm phản ứng trên
Bài 7. Dùng cách thức hóa học để phân biệt những chất khí sau:
a. H2, NH3, O2 và khí CO2
b. SO2, teo và khí N2
Bài 8. Làm thay nào để tách bóc được khí CO2 với O2 thành từng hóa học khí riêng biệt biệt.
Bài 9. Xem thêm: Dinh Dưỡng Trong Thịt Bò - Thịt Bò Chứa Bao Nhiêu Protein
A. 6. 1023 phân tử H2
B. 5,6 lít CH4 (đktc)
C. 6. 1023 phân tử H2
D. 1,5 g NH4Cl
Chọn cách thực hiện đúng nhất.
Bài 10. Người ta pha trộn được 24 g đồng bằng cách dùng hiđro nhằm khử đồng (II) oxit.
a. Cân nặng đồng (II) oxit bị khử là:
A. 15 g B. 45 g C. 60 g D. Tác dụng khác.
b. Thể tích hiđro (đktc) đã cần sử dụng là:
A.8,4 lít B. 12,6 lít C. 4,2 lít D. Công dụng khác
Chọn phương pháp đúng nhất.
Bài 11. Cho 13 g kẽm công dụng với 0,3 mol axit HCl thì thu được:
a. Cân nặng Zn
Cl2 là:
A. 20,4g B. 47g C. 40 g D. 18,5g
b. Thể tích hiđro (đktc) chiếm được là:
A. 3 lít B. 3,36 lít C. 4,48 lít D. 5,6 lít
Bài 12.
a. Mang lại 6 gam magie tính năng với dung dịch H2SO4. Hãy cho thấy thêm thể tích khí hiđro có mặt ở đktc ?
b. Nếu sử dụng thể tích H2 làm việc trên để khử 32 g fe (III) oxit thì thu được từng nào gam sắt?
Bài 13. Cho 7,5 gam láo hợp tất cả Al với Mg chức năng với dung dịch HCl.
a. Hãy tính khối lượng hỗn thích hợp muối khan nhận được sau phản nghịch ứng. Biết nhôm chỉ chiếm 36% trong tất cả hổn hợp ban đầu.
b. Tính thể tích hiđro (đktc) thu được nghỉ ngơi trên?
Bài 14. Cho 35,4 g hỗn kim loại tổng hợp loại có Fe, Zn tác dụng với dung dịch axit HCl thì thu được 13,44 lít H2 (đktc). Tính khối lượng mỗi kim loại.
Bài 15. Để khử hoàn toàn 68 g các thành phần hỗn hợp oxit sắt kẽm kim loại gồm Cu
O và Fe2O3 thì buộc phải dùng 25,76 lít H2 (đktc). Tính yếu tắc % về trọng lượng của mỗi oxit trong láo lếu hợp.
LỜI GIẢI VÀ ĐÁP ÁN
Bài 1. Học sinh tự viết PTHH
Chất oxi hóa: O2; Fe2O3; CO2; H2O
Chất khử : CO; Al; Mg
Bài 2.
Phi kim: S; P
Kim loại: Fe, Na
Oxit axit: P2O5; SO3
Oxit bazơ: Ca
O
Bazơ: KOH; Cu(OH)2
Muối: Na
HCO3; KNO3
Bài 3.
Đáp án A
Bài 4. Học sinh từ viết phương trình
Bài 5. Học sinh từ viết phương trình hóa học
Bài 6.
Đáp án E
Bài 7.
a. Đáp án:
B1: Than hồng → O2 (than bùng cháy rực rỡ ); CO2 (than tắt)
B2: Quì ẩm → NH3 (xanh quì tím ẩm)
Còn lại: H2
b. Đáp án:
B1: dd brom → SO2 (mất màu hỗn hợp bromo)
B2: Cu
O → teo (oxit đồng từ black chuyển sang color đỏ)
Còn lại là khí N2
Bài 8.
Các cách thực hiện: Đưa hỗn hợp qua nước vôi vào dư → CO2 bị giữ lại, bội nghịch ứng chế tác kết tủa còn O2 đi ra → lọc kết tủa nung chiếm được CO2









