Khi học tập sang phần dẫn xuất hiđrocacbon, có nghĩa là học về những hợp hóa học hữu cơ bao gồm nhóm chức thì đặc điểm của chúng càng đa dạng chủng loại hơn nữa. Bởi vì vậy, sẽ giúp đỡ các em khối hệ thống hóa kiến thức Kiến Guru sẽ Tổng hợp kỹ năng hóa 11 phần dẫn xuất hiđrocacbon một phương pháp ngắn gọn gàng và không thiếu thốn nhất.
Bạn đang xem: Tổng hợp kiến thức hóa 11
I. Tổng hợp kiến thức hóa 11: ANCOL
1. Định nghĩa, đồng đẳng, đồng phân, danh pháp:
- Ancol là phần lớn hợp chất hữu cơ vào phân tử gồm nhóm hiđroxyl -OH link trực tiếp cùng với nguyên tử C no.
- Phân loại:
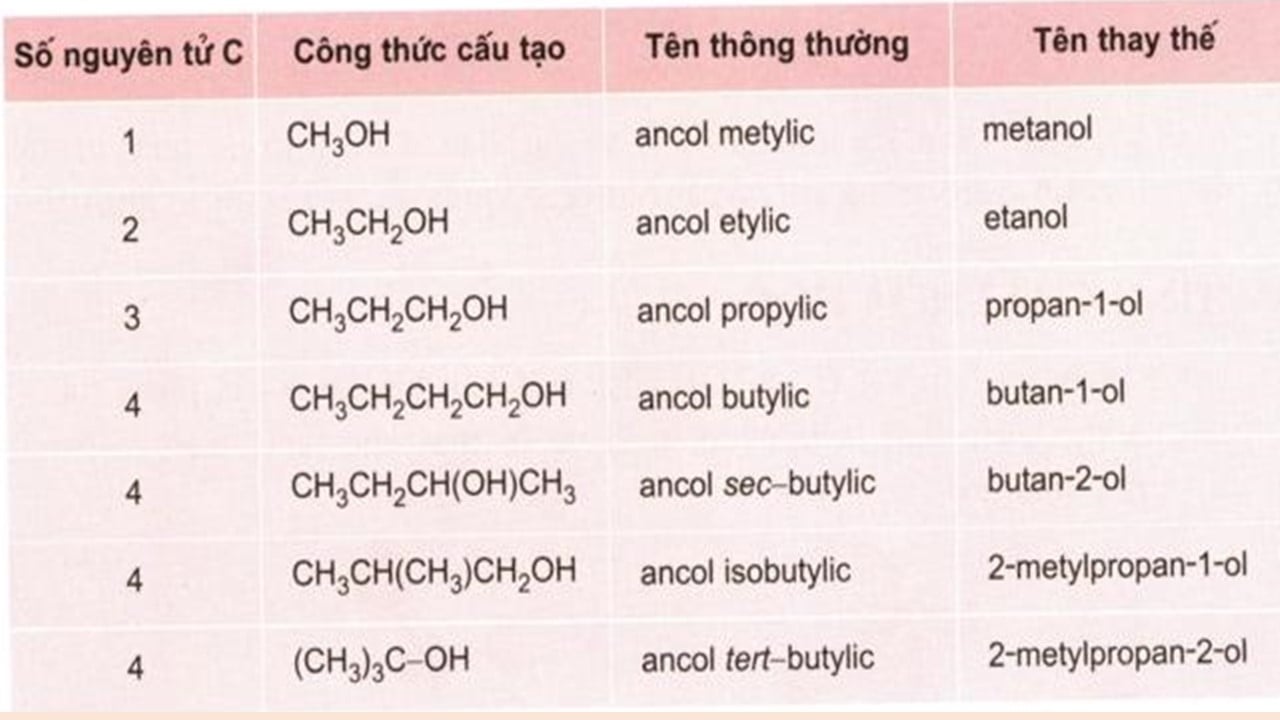
Tổng hợp kiến thức hóa 11
- một số trong những ancol mang tên riêng buộc phải nhớ:
CH2OH – CH2OH: Etilen glicol
CH2OH – CHOH – CH2OH: Glixerol
CH3 – CH(CH3) – CH2 – CH2 – OH: ancol amylic.
2. đặc thù vật lý:
+ Tan những trong nước bởi vì tạo được links hiđro với nước.
+ ánh sáng sôi của ancol cao hơn nữa so với các hiđrocacbon bao gồm cùng phân tử khối do có liên kết hiđro liên phân tử.
So sánh nhiệt độ sôi: muối > Axit > Ancol > Anđehit > Hiđrocacbon, ete cùng este...
Giải thích: ánh sáng sôi của một chất thường nhờ vào vào các yếu tố:
+ M: M càng bự thì ánh nắng mặt trời sôi càng cao.
+ Độ phân rất của liên kết: liên kết ion > liên kết cộng hóa trị phân rất > links cộng hóa trị ko phân cực.
+ Số link hiđro và thời gian chịu đựng của links hiđro.
3. đặc điểm hóa học:
4. Điều chế
II. Tổng hợp kỹ năng hóa 11: PHENOL
1. Định nghĩa, đồng đẳng, đồng phân, danh pháp:
- Phenol là đa số hợp hóa học hữu cơ vào phân tử tất cả nhóm -OH links trực tiếp cùng với nguyên tử C vòng benzen.
- CTTQ: Cn
H2n-6O (n ≥ 6)
- Phân nhiều loại :
+ Phenol 1-1 chức: Phân tử có một đội nhóm –OH phenol.
+ Phenol đa chức: Phân tử đựng hai hay những nhóm –OH phenol.
- Đồng phân
+ phương pháp tính nhanh: 3n-6(6
+ Áp dụng: C7H8O: 37-6 = 3 đồng phân.
2. Tính chất vật lý:
- Phenol là chất rắn, ko màu, rét chảy ở ánh nắng mặt trời 43o
C. Để lâu có màu hồng bởi bị oxi hóa.
- Phenol ít tan trong nước lạnh, tan nhiều hơn thế nữa trong nước nóng.
- Phenol tan nhiều trong rượu, ete, clorofom, …
- Phenol độc, bao gồm tính gần kề trùng, làm rộp da.
3. Tính chất hóa học:
4. Điều chế phenol:
- so sánh ancol – phenol:
III. Tổng hợp kỹ năng và kiến thức hóa 11: ANĐEHIT
1. Định nghĩa, đồng đẳng, đông phân, danh pháp:
- Anđehit là hợp hóa học hữu nhưng mà phân tử gồm nhóm –CH=O links trực tiếp cùng với nguyên tử cacbon hoặc nguyên tử hiđro.
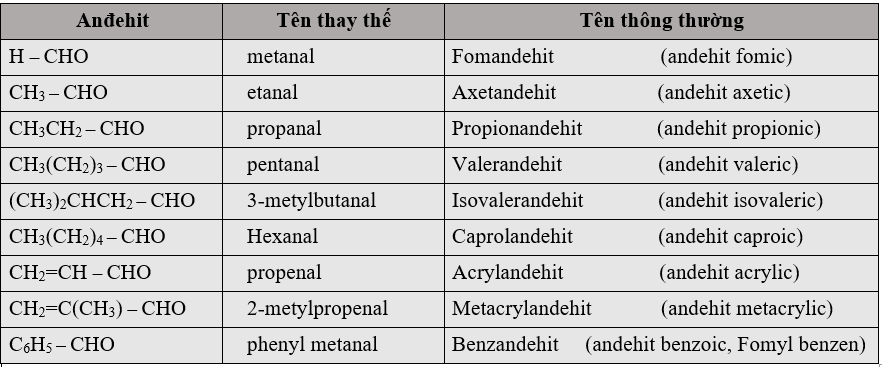
Tổng hợp kiến thức và kỹ năng hóa 11
2. đặc điểm vật lí:
- các anđehit đầu dãy là chất khí, tan nhiều trong nước. Các anđehit tiếp theo sau là lỏng hoặc rắn, độ tan giảm dần.
- hỗn hợp nước của anđehit fomic gọi là fomon. Hỗn hợp bão hòa của anđehit fomic (37 – 40%) hotline là fomalin.
3. đặc điểm hóa học:
4. Điều chế:
IV. Tổng hợp kiến thức hóa 11: XETON
1. Định nghĩa:
2. đặc điểm hóa học:
3. Điều chế:
V. Tổng hợp kỹ năng hóa 11: AXIT CACBOXYLIC
1. Định nghĩa, phân loại, danh pháp:
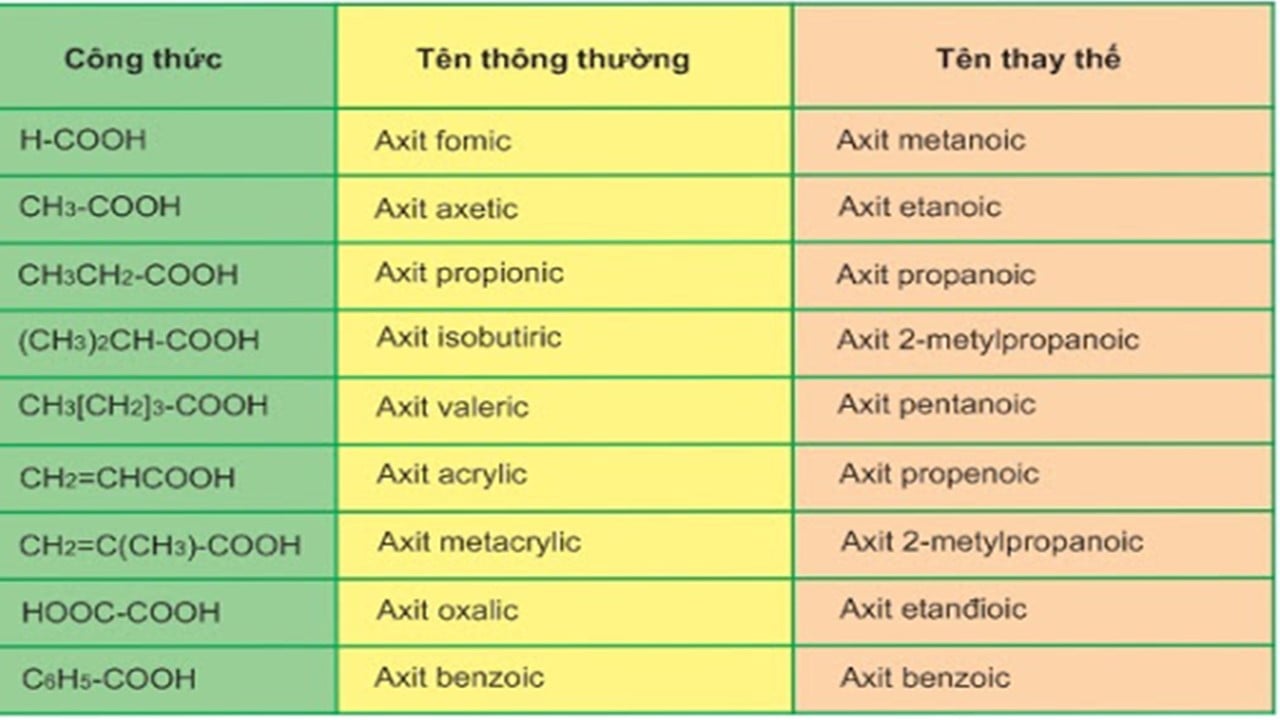
Tổng hợp kiến thức hóa 11
2. Tính chất vật lí:
- Là hóa học lỏng hoặc rắn ở ánh sáng thường.
- Tan tốt trong nước, độ tan giảm dần theo hướng tăng phân tử khối.
- ánh sáng sôi của axit > ancol (có cùng số C).
3. đặc thù hóa học:
4. Điều chế:
Mong rằng với những kiến thức Tổng hợp kỹ năng hóa 11 phần dẫn xuất hiđrocacbon đã hỗ trợ những kỹ năng bổ ích, giao hàng tốt cho quá trình học tập của các em.
Hóa 11 là công tác hóa nặng độc nhất trong 3 năm cấp cho 3. Vày nó có cả hữu cơ cùng vô cơ. Bởi vì đó, các bạn học sinh ước ao chọn môn hóa có tác dụng môn thi đh thì rất cần được có chiến lược và cách thức học tập mang đến phù hợp. Hôm nay, Trung trung ương gia sư WElearn sẽ chia sẻ cho bạn toàn bộ các cách học tốt hóa 11 để giúp bạn lựa chọn phương pháp phù hợp độc nhất vô nhị với phiên bản thân nhé!
1. Tổng hợp kỹ năng hóa 11
Chương Sự điện liChương đội Nitơ, Photpho
Chương nhóm Cacbon, Silic
Chương Đại cưng cửng về hóa học hữu cơ
Chương Hidrocacbon no
Chương Hidrocacbon không no
Chương Hidrocacbon thơm
Chương Dẫn xuất Halogen, Ancol, Phenol
Chương Anđehit, Xeton, Axit Cacboxylic
2. Cầm tắt các công thức hóa 11
2.1. Chương 1
2.1.1. Độ năng lượng điện li
Trong đó:
n là số phân tử phân li ra ion;no là tổng thể phân tử hòa tan.2.1.2. Hằng số phân li axit (Ka)Xét ví dụ: CH3COOH


Xét ví dụ: NH3 + H2O


KH2O =
H
Quy ước:
H M. Nếu như
M thì p
H = a.
Công thức: p
H = -log
Hoặc p
H = 14 + log
H và môi trườngp
H = 7: Môi ngôi trường trung tính;p
H p
H > 7: môi trường thiên nhiên bazơ.
2.2. Chương 2
2.2.1. Tính số mol HNO3 cần dùng làm hòa tan lếu láo hợp các kim loạin
HNO3 = 4n
NO + 2n
NO2 + 10n
N2O +12n
N2 +10n
NH4NO3
Lưu ý:
Không tạo ra khí làm sao thì số mol khí đó bằng 0.Giá trị nHNO3 không nhờ vào vào số kim loại trong láo hợp.Công thức này chỉ dùng khi cho hỗn kim loại tổng hợp loại tính năng với HNO3.Chú ý khi công dụng với Fe3+ vì fe khử Fe3+ về Fe2+ yêu cầu số mol HNO3 đã dùng làm hoà rã hỗn hợp kim loại nhỏ tuổi hơn so với tính theo phương pháp trên. Chính vì như thế phải nói rõ HNO3 dư bao nhiêu %.2.2.2. Tính cân nặng muối nitrat sắt kẽm kim loại thu được khi đến hỗn hợp các kim loại chức năng HNO3 (không bao gồm sự tạo nên thành NH4NO3):
mmuối = m
KL + 62.(3n
NO + n
NO2 + 8n
N2O +10n
N2)
Lưu ý:
Không tạo thành khí nào thì số mol khí đó bởi 0.Nếu tất cả sự chế tạo ra thành NH4NO3 thì cộng thêm vào mNH4NO3 có vào dd sau phản bội ứng.2.2.3. Tính năng suất phản ứng tổng hòa hợp NH3:
Nếu triển khai tổng thích hợp NH3 từ lếu hợp có N2 và H2 với tỉ lệ mol tương xứng là 1:3 thì năng suất tổng hợp là:
H% = 2 – 2.Mx/My
Với X là hỗn hợp thuở đầu và Y là các thành phần hỗn hợp sau.
2.2.4. Bài toán cho P2O5 hoặc H3PO4 vào dung dịch kiềmĐặt T = n
OH/n
H3PO4
Nếu:
T ≤ 1: tạo ra muối H2PO4-T = 2: chế tạo ra muối HPO4-T ≥ 3: tạo ra muối PO43-1 2PO4- và HPO42-2 42- và PO43-2.3. Chương 3
Bài toán dẫn khí CO2 vào hỗn hợp kiềm
Đặt T = n
OH / n
CO2
Chú ý:
mbình tăng = mchất hấp thụ
Nếu sau bội phản ứng bao gồm kết tủa:
mdd tăng = mchất hấp thụ – mkết tủamdd giảm = mkết tủa – mchất hấp thụ2.4. Chương 4
2.4.1. Tính độ bất bão hòa (k)Xét thích hợp chất: Cx
Hy
Oz
Nt
Xv (với X là những nguyên tố đội halogen)
Độ bất bão hòa

Xét thích hợp chất: Cx
Hy
Oz
Nt (a gam)

Trong đó:

Giả sử hợp chất hữu cơ gồm dạng: Cx
Hy
Oz
a/ phụ thuộc vào thành phần phần trăm khối lượng các nguyên tố:
Cx
Hy
Oz → x
C + y
H + z
O
M(g) 12x y 16z
100% %C %H %O
Ta bao gồm tỉ lệ:

b/ trải qua công thức đơn gián duy nhất (CTĐGN)
Từ CTĐGN ta có CTPT là (CTĐGN)n.
Xem thêm: Làm Sao Để Đổi Mật Khẩu Facebook Trên MáY TíNh Và ĐiệN ThoạI Đơn Giản
Để xác minh giá trị n ta dựa vào khối lượng mol phân tử M.
c/ Tính trực tiếp theo trọng lượng sản phẩm cháy:
Ta có phản ứng cháy :
Cx
Hy
Oz +(x + y/4 – z/2)O2 -> x
CO2 + H2O
(A)
Ta có:
x = n
CO2/n
A; y = 2n
H2O/n
A
Và: 12x + y + 16z = MA
Giải hệ trên ta được các giá trị x, y, z.
2.5. Chương 5
2.5.1. Công thức bao quát của ankanCn
H2n + 2 (n ≥ 1)
Cn
H2n (n ≥ 3)
2n – 4 + 1 (điều kiện: 3
2.5.4. Công thức tương quan đến bội phản ứng đốt cháy ankan:
Số mol ankan:

Số cacbon vào ankan:

Xét bội nghịch ứng tổng quát:

Hoặc

→Từ ankan ban đầu, sau phản bội ứng rất có thể thu nhiều chất sản phẩm.
Bảo toàn khối lượng: mtrước = msau

2.6. Chương 6
Công thức tổng thể của anken: CnH2n (n ≥ 2)Công thức tổng quát của ankađien: Cn
H2n -2 (n ≥ 3)Công thức bao quát của ankin: Cn
H2n – 2 (n ≥ 2)Công thức liên quan đến bội nghịch ứng đốt cháy ankađien hoặc ankin:

Số mol ankin hoặc ankađien:

Số cacbon vào ankin hoặc ankađien:

2.7. Chương 7
Dãy đồng đẳng benzen: CnH2n-6 (n ≥ 6)Số đồng phân đồng đẳng benzen: (n – 6)2 (điều kiện: 7 ≤ n ≤ 9)
2.8. Chương 8
Công thức ancol no, đơn chức, mạch hở: CnH2n +1OH (hoặc Cn
H2n+2O) (điều kiện: n ≥ 1).Công thức bao quát của ancol đa chức:Cx
Hy
Oz (điều kiện: x, y, z trực thuộc N*; y chẵn; 4 ≤ y ≤ 2x + 2; z ≤ x): hay được dùng khi viết phản bội ứng cháy.Cx
Hy(OH)z hay R(OH)z: hay được sử dụng khi viết làm phản ứng xảy ra ở team – OH.Cn
H2n +2 – 2k – z (OH)z ( với k = số link pi + vòng; z ≤ n).Tính số đồng phân ancol 1-1 chức no:Số đồng phân ancol Cn
H2n+2O = 2n-2 (điều kiện: 1 Tính số C của ancol no dựa vào phản ứng cháy:Số C của ancol no = n
CO2/(n
H2O – n
CO2)Tính số đồng phân ete no, 1-1 chức hở Cn
H2n+2O (n ≥ 2)Số đồng phân = (n-1)(n-2)/2Số ete tạo bởi hỗn vừa lòng n ancol 1-1 chức:Số ete =n(n+1)/2
2.9. Chương 9
Công thức bao quát của anđehit no, solo chức, hở: CxH2x +1CHO (x ≥ 0) hoặc Cn
H2n
O (n ≥ 1).Công thức bao quát của xeton no, 1-1 chức, hở: Cn
H2n
O (n ≥ 3)Công thức tổng thể của axit cacboxylic no, solo chức, mạch hở: Cx
H2x+1COOH (x ≥ 0) hoặc Cn
H2n
O2 (n ≥ 1).Tính số đồng phân anđehit đơn chức no:Số đồng phân anđehit Cn
H2n
O = 2n-3 (điều kiện: 2

Tính số đồng phân axit cacboxylic đơn chức no:Số đồng phân axit Cn
H2n
O2 = 2n-3 (điều kiện: 2 Tính số đồng phân este 1-1 chức no:Số đồng phân este Cn
H2n
O2 = 2n-2 (điều kiện: 1 Tính số đồng phân xeton 1-1 chức no:Số đồng phân xeton Cn
H2n
O = 1/2(n-2)(n-3) (điều kiện: 2
3. Hóa hữu cơ tốt hóa vô cơ khó khăn hơn?
Ở lịch trình lớp 11, bạn sẽ học 2 phần
Hóa vô cơ: được học phân tích chuyên sâu về đặc điểm hóa học và những dạng bài xích tập. Vày vậy, để học giỏi phần này, bạn phải học tốt lý thuyết và các định luật liên quan để nắm rõ phần này.Hóa hữu cơ: học về các hợp hóa học hữu cơ, biện pháp điều chế và các bài tập liên quan. Hầu hết các bạn học sinh hầu hết sợ phần này bởi vì bị rối giữa 2 phần hữu cơ và vô cơ. Mặc dù nhiên, dù ao ước hay không, chúng ta cũng đề nghị học vì đó là những loài kiến thức nền tảng để bạn học lên 12 với thi đại học.4. Cách học giỏi môn hóa lớp 11
4.1. Nắm vững lý thuyết
Nắm vững kiến thức định hướng là nhân tố tiên quyết để đổi mới một học sinh xuất sắc hóa. Bởi Hóa không đối kháng thuần chỉ nên môn bài xích tập mà lại nó còn có cả lượng loài kiến thức lý thuyết không hề ít. Do đó, bạn cần nắm dĩ nhiên lý thuyết để triển khai tốt các bài tập liên quan.
Hơn cầm cố nữa, so với các đề thi đại học, phần lý thuyết lúc nào thì cũng nhiều với dễ đem điểm hơn bài xích tập. Lúc vững lý thuyết, các bạn sẽ giải quyết và ăn điểm những câu kim chỉ nan một phương pháp nhanh chóng, dành riêng thời gian để gia công các câu khó khăn hơn.
4.2. Làm nhiều bài xích tập
Làm bài tập là cách để giúp chúng ta hiểu bài bác nhanh nhất. Học định hướng không thì quan yếu hiểu với chắc kỹ năng được. Do vậy, bạn phải làm thêm nhiều bài bác tập để hiểu rõ hơn.
Hơn nữa, lúc làm bài tập cũng chính là lúc bạn phân biệt mình mơ hồ nước ở mảng kiến thức nào, khó khăn hiểu ở đâu. Trường đoản cú đó rất có thể đưa ra hướng giải quyết để cải thiện.
Việc làm bài xích tập nhiều để giúp bạn cải thiện khả năng tư duy và áp dụng hơn. Lúc tiếp xúc với rất nhiều dạng bài bác tập, cho lúc làm bài xích kiểm tra, bạn sẽ tự tin rộng để giải quyết và xử lý những bài xích “khó nhằn”.
4.3. Kiên trì
“Có công mài sắt gồm ngày thành công”. Kiên định là yếu đuối tố để giúp bạn đổi thay một học tập sinh giỏi hóa tuy vậy bạn có thông minh giỏi không. Chỉ việc bạn đủ kiên trì và thế gang91, các bạn sẽ thành công.
Việc bền chí nỗ lực, cần cù làm các bài tập thường xuyên xuyên để giúp bạn cải thiện kiến thức cũng tương tự các kỹ năng của mình. Trường đoản cú đó, việc tư duy của người sử dụng cũng trở nên nhạy bén hơn.
4.4. Tập trung lắng nghe giáo viên
Không ai rất có thể giỏi nếu không nghe cô giáo giảng bài. Đồng ý rằng bạn có thể tự học tập được. Mà lại nếu tự học không có sự gợi ý của thầy giáo thì sẽ khá khó để tiến bộ.
Khi lắng nghe gần như gì thầy cô dạy ở lớp sẽ giúp bạn biết được mình không rõ nơi nào và hỏi lại ngay. Tránh tình trạng để lâu cùng mất gốc.
Bạn đề xuất rèn luyện cách biểu hiện học tập tích cực bằng phương pháp thường xuyên trao đổi, bàn bạc để mang lại tiết học thêm sinh động, bớt nhàm chán. Dựa vào đó, tinh thần của bạn cũng thấy thoải mái, bớt căng thẳng hơn với học tập công dụng hơn.
4.5. Tự học tập ở nhà
Thực tế, 1 tuần chỉ gồm từ 2 – 3 huyết hóa thì cấp thiết nào thầy cô đáp ứng được kỹ năng một cách vừa đủ và trọn vẹn. Vày vậy, chúng ta nên dành thời hạn ở nhà của bản thân mình để từ bỏ học với tìm tòi thêm hầu như thứ new để học tốt hơn.
Việc ôn lại các kiến thức tại nhà để giúp đỡ bạn nhớ bài bác lâu hơn. Đặc biệt là có thời hạn để khám phá kỹ lại phần đông phần bản thân hổng kiến thức để “lấp đầy” nó.
4.6. Chế tạo niềm đắm say với hóa học
Để học tốt hóa, bắt buộc bạn phải gồm niềm đam mê với nó. Vị chỉ bao gồm khi thực sư đam mê, các bạn mới không còn mình dốc sức mang lại nó.
Bạn càng chán ghét môn hóa thì câu hỏi tiếp thu nó càng khó. Vày vậy, hãy bình tĩnh, gạt quăng quật những “căm ghét” đó qua 1 bên, làm chúng ta với nó, bạn sẽ thấy nó dễ dàng thở hơn biết nhường nhịn nào.
4.7. Chuẩn bị bài trước lúc tới lớp
Chuẩn bị bài bác trước khi tới trường cũng là cách giúp cho bạn học tốt môn hóa 11. Khi chúng ta có thái độ sẵn sàng, các bạn sẽ học nó một bí quyết tự tin và dễ chịu hơn.
Hơn nắm nữa, việc sẵn sàng bài trước khi tới trường cũng là phương pháp để bạn diễn đạt ý thức tiếp thu kiến thức của mình. Khi đó, thầy cô sẽ đánh giá cao bạn hơn với dĩ nhiên, bạn cũng trở thành có tuyệt hảo tốt cùng với thầy cô hơn.
Ngoài ra, khi xem bài trước khi tới lớp, chúng ta cũng có thể nắm được những kỹ năng cơ phiên bản trước, lúc đến lớp nghe thầy cô giảng bài, bạn sẽ dễ “bắt nhịp” và phát biểu hơn.
4.8. Học tập nhóm
Dù là môn nào đi nữa thì câu hỏi học theo nhóm cũng chính là một phương pháp cực kỳ kết quả để nâng cao kiến thức của mình. Vì khi học theo nhóm, đều người giúp sức lẫn nhau. Những cái đầu lúc nào thì cũng hơn một chiếc đầu. Ai biết phần như thế nào chỉ phần đó sẽ cùng giúp nhau văn minh hơn.

Hơn vậy nữa, trong quy trình học, sẽ có tương đối nhiều bạn không đủ anh dũng để hỏi lại thầy cô. Lúc này, học team là giải pháp tốt tốt nhất giúp các bạn cũng có thể giải đáp những thắc mắc của mình.
Ngoài ra, đối với các bạn giỏi, học theo nhóm cũng là bí quyết để các bạn ôn và khám nghiệm lại kỹ năng của mình, coi mình có thực sự hiểu bài bác hay không. Nếu như bạn hiểu bài, câu hỏi giảng bài cho những người khác hiểu sẽ tương đối dễ dàng.
4.9. Nắm những quy tắc giải nhanh
Đối với chương trình hóa cấp cho 3 nói thông thường và của lớp 11 nói riêng, hầu hết chúng ta đều thi trắc nghiệm. Vì vậy, khi tải cho mình những công thức nhanh sẽ giúp đỡ bạn giải quyết và xử lý bài toán 2 trang chỉ vào 2 phút.
Tuy nhiên, lúc áp dụng các quy tắc này, bạn cần nắm rõ thực chất của nó. Nếu như không, bạn sẽ sử dụng nó một phương pháp mơ hồ nước và rất đơn giản lẫn lộn chúng với nhau. Khi đó, số đông thứ vẫn phản tính năng đấy.
Quan trọng, mặc dù có những công thức nhanh, các bạn cũng nên biết phương pháp giải từ luận của nó để ví như “lỡ” tất cả quên, chúng ta có thể “mò” lại được.
Như vậy, WElearn sẽ Hé Lộ tất cả Cách Học tốt Hóa học tập Lớp 11 tác dụng Nhất. Hy vọng chúng ta có thể áp dụng các phương thức trong bài viết này nhằm “làm chủ” môn hóa của chính mình nhé. Chúc chúng ta thành công!
? Trung trọng tâm gia sư WElearn siêng giới thiệu, cung cấp và làm chủ Gia sư.? Đội ngũ Gia sư với trên 1000 gia sư được kiểm xem xét kỹ càng.? tiêu chuẩn của shop chúng tôi là cấp tốc CHÓNG và HIỆU QUẢ. Cấp tốc CHÓNG có Gia sư cùng HIỆU QUẢ trong giảng dạy.









